¿A qué hora se anuncia la FDA??
E-left-2-solid “width =” 32 “altura =” 32 “] ¿Cuántos medicamentos aprueba la FDA cada año? El número de nuevas aprobaciones de medicamentos por la FDA varía cada año. En los últimos años, la FDA ha aprobado un promedio de alrededor de 30 nuevos medicamentos anualmente.[/wpremark]
son aprobaciones de la FDA, las aprobaciones de la FDA permanentes para medicamentos no son permanentes. Después de aprobar un medicamento, la FDA continúa monitoreando su seguridad y efectividad a través de la vigilancia posterior al mercado. Si surgen nuevas preocupaciones de seguridad, la FDA puede tomar medidas regulatorias, incluida la modificación o retirada de la aprobación.
¿Cuánto tiempo lleva la FDA para aprobar un medicamento?. En promedio, la FDA tarda unos 10 meses en revisar y tomar una decisión sobre una solicitud de drogas estándar. Sin embargo, las rutas aceleradas como la revisión de prioridad pueden acortar la línea de tiempo a alrededor de 6 meses.
¿Cuál es el proceso para la aprobación del medicamento de la FDA? El proceso para la aprobación del medicamento de la FDA implica varias fases. Primero, está la fase de descubrimiento y desarrollo, seguida de investigación preclínica y ensayos clínicos. Una vez que se completan estos pasos, se presenta una nueva solicitud de medicamento (NDA) a la FDA para su revisión. Si la FDA determina que los beneficios del medicamento superan los riesgos, otorgará la aprobación.
¿Puede la FDA rechazar un medicamento después de la aprobación en algunos casos, la FDA puede retirar o suspender la aprobación de un medicamento después de que se haya otorgado. Esto generalmente ocurre si surgen nuevas preocupaciones de seguridad o si estudios adicionales indican que el medicamento no es tan efectivo como se creía inicialmente. La FDA tiene la autoridad de tomar medidas regulatorias para proteger la salud pública.
¿Cómo puedo conocer los retiros de medicamentos de la FDA?. Puede visitar la página de retiros de la FDA, retiros del mercado y alertas de seguridad para buscar retiros de medicamentos específicos. Además, puede registrarse para obtener notificaciones por correo electrónico de la FDA para recibir actualizaciones sobre retiros de medicamentos y otras alertas de seguridad.
¿Puede la FDA aprobar medicamentos para uso fuera de etiqueta, la FDA no regula ni controla la práctica de la medicina, incluido el uso de medicamentos aprobados para fines no etiquetados. Una vez que se aprueba un medicamento, los proveedores de atención médica pueden recetarlo para afecciones o poblaciones de pacientes que no se especifican en el etiquetado aprobado. Sin embargo, el fabricante no puede promover el medicamento para usos fuera de etiqueta.
¿Con qué frecuencia se reúne la FDA para revisar las solicitudes de medicamentos? El proceso de revisión de la FDA para aplicaciones de medicamentos ocurre de manera continua. No hay un horario específico para cuándo se reúne la FDA para revisar las solicitudes. En cambio, la FDA ha establecido plazos de revisión basados en el tipo de revisión designada para la aplicación, como revisión de prioridad o revisión estándar.[/wprem
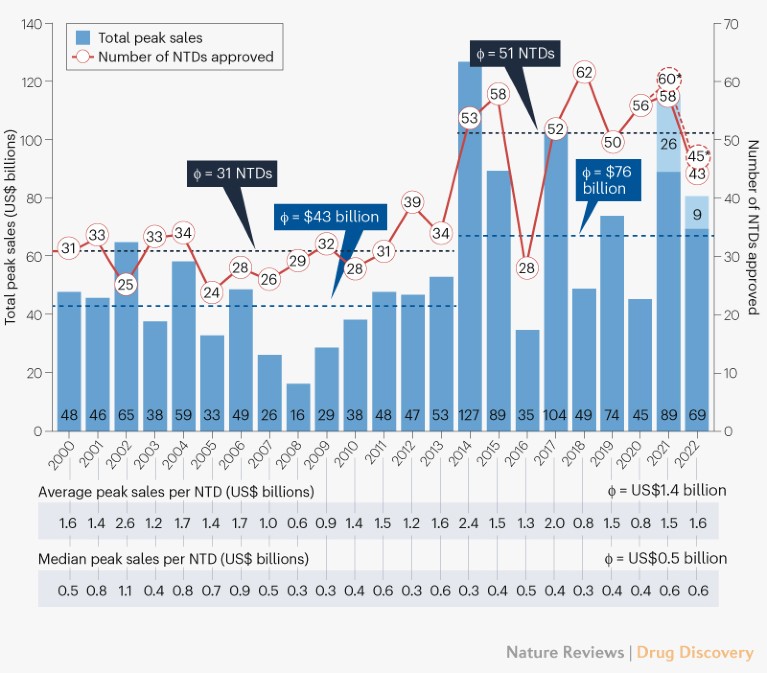
Notas: Antes de que el mercado se abra para los anuncios publicados antes de las 9:30 ET de las fechas de anuncios de la FDA; durante las horas del mercado para los anunciados de 9:30 a 16:00 ET; Después del cierre del mercado para las notificaciones de la FDA ocurrió después de las 16:00 ET de las fechas de anuncio o un par de días después de las fechas de anuncio de la FDA.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿La FDA alguna vez aprueba temprano?
La FDA instituyó su programa de aprobación acelerado para permitir la aprobación anterior de los medicamentos que tratan las afecciones graves y satisfacer una necesidad médica no satisfecha basada en un punto final sustituto.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Cuál es la línea de tiempo para la aprobación acelerada de la FDA?
Revisión prioritaria
Una línea de tiempo de revisión estándar es de aproximadamente diez meses. Sin embargo, bajo una designación de revisión de prioridad, la FDA revisa la aplicación durante seis meses. Este tipo de aprobación acelerada se centra en la evaluación de los medicamentos.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Cuál es el tiempo para que la FDA dé la aprobación de los medicamentos?
La fase de ensayo clínico puede tardar años en completarse. Sin embargo, una vez que la investigación ha demostrado que el medicamento es seguro y útil, la FDA generalmente revisa y aprueba o niega una solicitud de un nuevo medicamento dentro de los 6 meses.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Cuáles son las 4 fases de aprobación de la FDA?
Descubra cómo la FDA está acelerando el proceso de aprobación.Nueva aplicación de drogas. Una nueva aplicación de drogas (NDA) cuenta la historia completa de una droga.Revisión de la FDA. Una vez que la FDA recibe un NDA, el equipo de revisión decide si está completo.Aprobación de la FDA.Comités asesores de la FDA.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Dónde puedo ver mis aprobaciones de la FDA?
Busque la droga en drogas @ FDA.
La mayoría de los medicamentos humanos aprobados por la FDA y los productos biológicos terapéuticos se enumeran en medicamentos @ FDA, una base de datos de búsqueda. La base de datos le permite buscar por nombre de drogas, ingrediente activo o número de aplicación (NDA, anda o bla).
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Cuáles son las 5 fases de aprobación de la FDA?
Información Forstep 1: Descubrimiento y desarrollo.Paso 2: Investigación preclínica.Paso 3: Investigación clínica.Paso 4: Revisión de drogas de la FDA.Paso 5: Monitoreo de seguridad de drogas posterior al mercado de la FDA.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Dónde puedo rastrear las aprobaciones de la FDA?
FDA -Track: Centro de Evaluación e Investigación de Drogas – Revisión de seguridad previa a la aprobación – Domance de medicamentos y biológicos.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Cuánto tiempo lleva la fase 3 de la aprobación de la FDA?
Tras la finalización exitosa de un ensayo de fase 3, se puede enviar una nueva solicitud de medicamento (NDA) a la FDA para solicitar revisión de aprobación. Luego, la FDA tardará de 6 a 10 meses en revisar todos los datos enviados y aceptar o negar el NDA.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] Cómo encontrar letras de la FDA 483
Los ejemplos de 483 recientemente emitidos están disponibles en la sala de lectura electrónica de Ora. Las preguntas sobre las observaciones de inspección pueden dirigirse por correo electrónico a [email protected].
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Por qué la FDA tarda tanto en aprobar las drogas?
Nuevos medicamentos están constantemente en desarrollo. Sin embargo, la Administración de Alimentos y Medicamentos (FDA) tiene protocolos de seguridad estrictos en los pasos que deben pasar los nuevos medicamentos antes de que las personas puedan usarlos.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Con qué frecuencia la FDA Fast Track
Los informes de aprobaciones de CDER Fast Track (FT) contienen una lista de aprobaciones para medicamentos designados por la vía rápida. Los nuevos informes se publicarán en enero, abril, julio y octubre de cada año (trimestral) a partir del 6-30-22.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Qué porcentaje de drogas pasan la fase 3?
La tasa de éxito de cada etapa de descubrimiento de drogas en la academia fue de 31.8% para preclínico, 75.1% para la fase I, 50.0% para la fase II, 58.6% para la fase III y 87.5% para NDA y BLA.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] Son 483 respuestas públicas
Teóricamente, el formulario FDA 483 son información pública y, por lo tanto, están disponibles a través de la Oficina de la Ley de Libertad de Información de la FDA. Entonces, cualquier formulario FDA 483 puede ser solicitado por cualquier persona. Dicho esto, solicitar un 483 puede ser costoso y puede llevar mucho tiempo.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Son públicas las cartas de aprobación de la FDA?
(e) Después de que la FDA envíe una carta de aprobación al solicitante, los siguientes datos e información en la solicitud o solicitud abreviada están disponibles de inmediato para la divulgación pública, a menos que el solicitante muestre que existen circunstancias extraordinarias.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Cuánto tiempo se tarda la aprobación de los medicamentos para lanzarse?
Medicamentos en los países desarrollados
Resultados: Se observó una gran variación en el tiempo de lanzamiento de todas las nuevas entidades moleculares (90 a 430 días) y el tiempo para reembolsar desde el lanzamiento en los países estudiados (90 a 540 días).
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Cuál es la tasa de éxito de la aprobación de la FDA?
La tasa de éxito de cada etapa de descubrimiento de drogas en la academia fue de 31.8% para preclínico, 75.1% para la fase I, 50.0% para la fase II, 58.6% para la fase III y 87.5% para NDA y BLA. El loa de la fase I a la aprobación fue de 19.3% (Figura 1).
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] Cuánto más rápido es la aprobación acelerada
Resumen ejecutivo. El ‘proyecto de confirmación’ del Centro de Excelencia de Oncology considera que si un ensayo confirmatorio está en curso en el momento de la aprobación acelerada, la conversión a la aprobación regular lleva un promedio de tres años versus 4.9 años si el juicio comienza después de AA.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Cuánto tiempo lleva la aprobación de la FDA después de la fase 3?
Tras la finalización exitosa de un ensayo de fase 3, se puede enviar una nueva solicitud de medicamento (NDA) a la FDA para solicitar revisión de aprobación. Luego, la FDA tardará de 6 a 10 meses en revisar todos los datos enviados y aceptar o negar el NDA.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Cuál es la tasa de éxito de la aprobación de la FDA después de la fase 3?
La tasa de éxito de cada etapa de descubrimiento de drogas en la academia fue de 31.8% para preclínico, 75.1% para la fase I, 50.0% para la fase II, 58.6% para la fase III y 87.5% para NDA y BLA. El loa de la fase I a la aprobación fue de 19.3% (Figura 1).
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] Lo que sucede después de que se emite un 483
Si la FDA encuentra inadecuada la respuesta 483 de una empresa, podría resultar en una carta de advertencia. Si se continúan ocurriendo problemas, incluso podría haber acciones adicionales, como enjuiciamiento o sanciones civiles. La acción más drástica que la agencia podría tomar es un decreto de consentimiento.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] Cuánto tiempo responder a la FDA 483
dentro de los 15 días hábiles
El Formulario 483 de la FDA no constituye una determinación de la agencia final y se alienta a las empresas a responder al Formulario 483 de la FDA por escrito con su plan de acción correctiva con documentación de apoyo dentro de los 15 días hábiles a partir de la emisión del Formulario FDA 483 e implementar el plan de acción correctiva expedentemente.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Cómo obtengo alertas de aprobación de la FDA?
Nuestro servicio de alerta de correo electrónico gratuito le permite recibir importantes noticias e información de la FDA a medida que estén disponibles. Para registrarse, seleccione los temas que le interesan. Para suscribirse, todo lo que necesita es una dirección de correo electrónico válida.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Cómo puedo acelerar mi proceso de aprobación de drogas?
La designación de la vía rápida debe ser solicitada por la compañía farmacéutica. La solicitud se puede iniciar en cualquier momento durante el proceso de desarrollo de fármacos. La FDA revisará la solicitud y tomará una decisión dentro de sesenta días en función de si el medicamento satisface una necesidad médica insatisfecha en una afección grave.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] Cuántas drogas fallan en la fase 3
Hwang et al. [58] evaluó 640 ensayos de fase 3 con nuevas terapias y descubrió que el 54% falló en el desarrollo clínico, con el 57% de los que fallaron debido a una eficacia inadecuada.


