¿Cuáles son las 4 fases de aprobación de la FDA??
Resumen del proceso de aprobación de la FDA
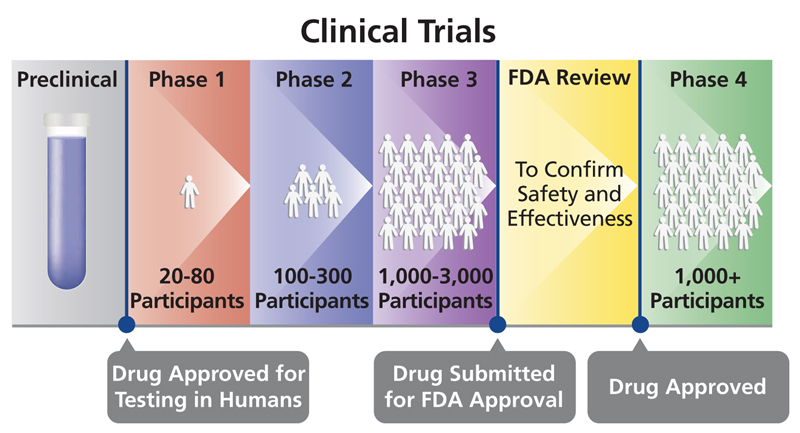
El proceso de aprobación de la FDA consta de cuatro fases principales:
1. Descubrimiento y desarrollo
2. Investigación preclínica
3. Investigación clínica
4. Revisión de drogas de la FDA
Este proceso es seguido por el monitoreo de seguridad de medicamentos posteriores al mercado de la FDA.
Preguntas frecuentes:
1. ¿Cuáles son las fases de la aprobación de la FDA??
Las fases de la aprobación de la FDA son: descubrimiento y desarrollo, investigación preclínica, investigación clínica, revisión de medicamentos de la FDA y monitoreo de seguridad de medicamentos después del mercado de la FDA.
2. ¿Cuál es el proceso de 5 pasos de un medicamento aprobado por la FDA??
El proceso de 5 pasos para la aprobación de la FDA de un medicamento incluye: descubrimiento/concepto, investigación preclínica, investigación clínica, revisión de la FDA y monitoreo de seguridad posterior al mercado de la FDA.
3. ¿Cuánto tiempo lleva la aprobación de la FDA después de la fase 3??
Después de completar con éxito los ensayos de fase 3, se puede enviar una nueva solicitud de drogas (NDA) a la FDA para su revisión. La FDA generalmente tarda de 6 a 10 meses en revisar los datos y tomar una decisión sobre la aprobación.
4. ¿Qué es la fase 3 de la aprobación de la FDA??
Los ensayos de fase 3 implican administrar el medicamento experimental a grandes grupos de personas. Se confirma su efectividad, se monitorean los efectos secundarios y las comparaciones con los tratamientos existentes se realizan para garantizar un uso seguro.
5. ¿Cuánto tiempo lleva la aprobación de la FDA después de la fase 2??
La duración del proceso de aprobación de la FDA varía según el tipo de solicitud presentada, que oscila entre una semana hasta ocho meses para el autorregistro, solicitud 510 (k) o solicitud de aprobación previa al mercado (PMA).
6. ¿Qué es la fase 3 vs aprobación de la FDA de fase 4??
La fase 3 es la fase final antes de la aprobación de la FDA, mientras que la fase 4 ocurre después de la aprobación e implica monitorear de cerca la eficacia y seguridad del tratamiento con un gran grupo de participantes.
7. ¿Cuánto tiempo tarda en estar disponible un medicamento después de la aprobación de la FDA??
La designación de revisión prioritaria tiene como objetivo acortar el tiempo de acción dentro de los seis meses para los medicamentos que mejoran significativamente el tratamiento, el diagnóstico o la prevención de afecciones graves, en comparación con el tiempo de revisión estándar de 10 meses.
8. ¿Cuánto tiempo tarda la FDA en aprobar una droga??
Después de completar ensayos clínicos que establecen la seguridad y la efectividad del medicamento, la FDA generalmente revisa y toma una decisión sobre una nueva aplicación de medicamentos dentro de los 6 meses.
9. ¿Se puede aprobar un medicamento sin la fase 3??
En ciertos casos, como los medicamentos contra el cáncer, la FDA puede otorgar la aprobación acelerada antes de completar los ensayos de fase 3.
10. ¿Qué es la aprobación de la FDA de la Fase 2??
Los estudios de fase 2 implican administrar el medicamento a pacientes con la enfermedad o afección objetivo. Estos estudios evalúan la efectividad e identifican los efectos secundarios y riesgos comunes a corto plazo.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Cuáles son las fases de la aprobación de la FDA?
Información Forstep 1: Descubrimiento y desarrollo.Paso 2: Investigación preclínica.Paso 3: Investigación clínica.Paso 4: Revisión de drogas de la FDA.Paso 5: Monitoreo de seguridad de drogas posterior al mercado de la FDA.
En caché
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Cuál es el proceso de 5 pasos de un medicamento aprobado por la FDA?
Una compañía farmacéutica que busca la aprobación de la FDA para vender un nuevo medicamento recetado debe completar un proceso de cinco pasos: descubrimiento/concepto, investigación preclínica, investigación clínica, revisión de la FDA y monitoreo de seguridad posterior al mercado de la FDA.
En caché
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Cuánto tiempo lleva la aprobación de la FDA después de la fase 3?
Tras la finalización exitosa de un ensayo de fase 3, se puede enviar una nueva solicitud de medicamento (NDA) a la FDA para solicitar revisión de aprobación. Luego, la FDA tardará de 6 a 10 meses en revisar todos los datos enviados y aceptar o negar el NDA.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Qué es la fase 3 de la aprobación de la FDA?
Pruebas de fase III
El medicamento o el tratamiento del estudio experimental se administra a grandes grupos de personas. Los investigadores confirman su efectividad, monitorean los efectos secundarios, la comparan con los tratamientos de uso común y recopilan información que permitirá que el medicamento o el tratamiento experimental se usen de manera segura.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Cuánto tiempo lleva la aprobación de la FDA después de la fase 2?
El proceso de aprobación de la FDA puede tomar entre una semana y ocho meses, dependiendo de si se autoinsegre, envíe una solicitud 510 (k) o envíe una solicitud de aprobación previa a la comercialización (PMA).
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Qué es la fase 3 vs aprobación de la FDA de fase 4?
La fase 3 es la fase final antes de que un tratamiento reciba la aprobación de la FDA. Después de la aprobación de la FDA, un tratamiento pasa por la fase 4. Esta fase involucra al grupo más grande de participantes. Puede durar varios años a medida que los investigadores continúan monitoreando la eficacia y la seguridad del tratamiento.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Cuánto tiempo tarda en estar disponible un medicamento después de una aprobación de la FDA?
La revisión prioritaria significa que la FDA tiene como objetivo tomar medidas en una solicitud dentro de los seis meses, en comparación con los 10 meses bajo la revisión estándar. Una designación de revisión de prioridad dirige la atención y los recursos para evaluar los medicamentos que mejorarían significativamente el tratamiento, el diagnóstico o la prevención de afecciones graves.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Cuánto tiempo tarda la FDA en aprobar una droga?
La fase de ensayo clínico puede tardar años en completarse. Sin embargo, una vez que la investigación ha demostrado que el medicamento es seguro y útil, la FDA generalmente revisa y aprueba o niega una solicitud de un nuevo medicamento dentro de los 6 meses.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Se puede aprobar un medicamento sin la fase 3?
La aprobación acelerada a menudo se usa para medicamentos contra el cáncer
La FDA también puede aprobar medicamentos contra el cáncer antes de que se realice un ensayo clínico de fase III. Este proceso se llama aprobación acelerada.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Qué es la aprobación de la FDA de la Fase 2?
En los estudios de la fase 2, los investigadores administran el medicamento a un grupo de pacientes con la enfermedad o condición para la cual se está desarrollando el medicamento. Por lo general, involucrando a unos cientos de pacientes, estos estudios no son lo suficientemente grandes como para mostrar si el medicamento será beneficioso.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Qué es la fase de la FDA?
La fase 2 incluye los estudios clínicos controlados realizados para evaluar la efectividad del medicamento para una indicación o indicaciones particulares en pacientes con enfermedad o condición en estudio y para determinar los efectos secundarios y riesgos comunes a corto plazo asociados con el medicamento.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Qué porcentaje de drogas pasan la fase 3?
La tasa de éxito de cada etapa de descubrimiento de drogas en la academia fue de 31.8% para preclínico, 75.1% para la fase I, 50.0% para la fase II, 58.6% para la fase III y 87.5% para NDA y BLA.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] Lo que viene después de las pruebas de fase 3
Después del ensayo de fase III, la FDA revisa los resultados del ensayo clínico para asegurarse de que el tratamiento sea seguro y efectivo para que las personas los usen. La FDA decide si aprueba el tratamiento para que esté disponible para todos los pacientes. Hay muchas preguntas frecuentes sobre los ensayos de fase III.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Qué es la fase 2 del proceso de aprobación de la FDA?
En los estudios de la fase 2, los investigadores administran el medicamento a un grupo de pacientes con la enfermedad o condición para la cual se está desarrollando el medicamento. Por lo general, involucrando a unos cientos de pacientes, estos estudios no son lo suficientemente grandes como para mostrar si el medicamento será beneficioso.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Cuántas drogas en la fase 3 se aprueban?
La tasa de éxito de cada etapa de descubrimiento de drogas en la academia fue de 31.8% para preclínico, 75.1% para la fase I, 50.0% para la fase II, 58.6% para la fase III y 87.5% para NDA y BLA.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] Cuántos ensayos antes de que se apruebe un medicamento
La FDA generalmente requiere la fase 1, 2 y 3 ensayos que se realizarán para determinar si el medicamento o el dispositivo puede ser aprobado para su uso posterior. Si los investigadores consideran que la intervención es segura y efectiva después de las tres primeras fases, la FDA la aprueba para uso clínico y continúa monitoreando sus efectos.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Con qué frecuencia la FDA niega la aprobación?
Tan recientemente como 2008, las compañías que presentan solicitudes para vender medicamentos nunca antes comercializados, a las que la FDA se hace referencia como “nuevas entidades moleculares”, enfrentó el rechazo el 66% del tiempo. Sin embargo, en lo que va del año, la FDA ha rechazado solo tres usos para nuevas entidades químicas, y aprobó 25, una tasa de aprobación del 89%.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Con qué frecuencia fallan las drogas en la aprobación de la FDA?
¿Por qué el 90% del desarrollo clínico de fármacos fallas solo 1 de cada 10 candidatos a los medicamentos aprueba con éxito las pruebas de ensayos clínicos y la aprobación regulatoria.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Cuánto tiempo se tarda en pasar una droga de la fase 2 a la fase 3?
La duración del estudio para los ensayos clínicos de fase 3 suele ser de 1 a 4 años.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Qué sucede si la droga tiene éxito en la fase 3?
Debido al mayor número de participantes y una mayor duración o fase III, los efectos secundarios raros y a largo plazo tienen más probabilidades de aparecer durante esta fase. Si los investigadores demuestran que el medicamento es al menos tan seguro y efectivo como otros que ya están en el mercado, la FDA generalmente aprobará el medicamento.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Qué enfatiza la fase 3 clínica del proceso de aprobación de medicamentos de la FDA?
Los estudios de fase 3 comienzan si se muestra evidencia de efectividad en la fase 2. Estos estudios recopilan más información sobre la seguridad y la efectividad, el estudio de diferentes poblaciones y las diferentes dosis y el uso del medicamento en combinación con otros medicamentos.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Qué fase fallan la mayoría de las drogas?
Fase III
Los estudios clínicos de la Fase II representan un punto crítico para determinar los costos de los medicamentos, y la Fase II es un mal predictor del éxito de los medicamentos: >El 30% de los medicamentos que ingresan a los estudios de fase II no pueden progresar, y >El 58% de las drogas fallan en la fase III.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] ¿Cuánto tiempo se tarda en obtener un ensayo clínico después de la fase 3?
Entre uno y cuatro años
Los ensayos de fase 2, que examinan la eficacia y los efectos secundarios de un tratamiento, generalmente duran varios meses a dos años. Los ensayos de fase 3, que examinan la eficacia de un tratamiento y monitorean las reacciones adversas, generalmente duran entre uno y cuatro años.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] Es la fase 3 la última fase
La fase 3 es la fase final antes de que un tratamiento reciba la aprobación de la FDA. Después de la aprobación de la FDA, un tratamiento pasa por la fase 4.
[wPremark_icon icon = “QUOTE-TE-SOT-2-SOLID” Width = “Width =” “” 32 “altura =” 32 “] Cuántas drogas pasan la fase 1
Una prueba de fase I tarda varios meses en completarse. Alrededor del 70 por ciento de los medicamentos experimentales pasan esta fase inicial de las pruebas.


